




引言
外泌体作为细胞间通讯的重要媒介,在维持生理平衡和疾病发生发展中扮演着关键角色。免疫细胞和干细胞作为两类重要的细胞群体,其分泌的外泌体在免疫调节、组织修复和再生医学等领域展现出巨大的潜力。然而,由于细胞类型和功能的不同,这两类外泌体在组成、功能和临床应用上存在显著差异。
文献揭示:
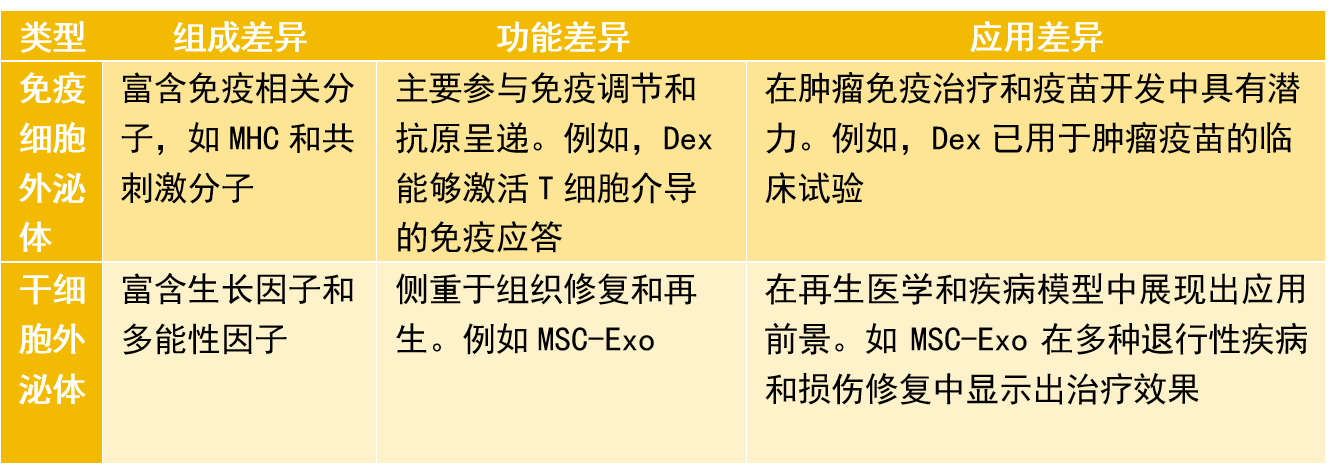
(1) 免疫细胞外泌体富含免疫相关分子,主要参与免疫调节和抗原呈递,在肿瘤免疫治疗和疫苗开发中具有潜力。
(2) 干细胞外泌体富含生长因子和多能性因子,通过促进血管生成、抑制炎症和纤维化,参与组织修复和再生。在再生医学和损伤修复的临床中展现出应用前景。
想象一下,如果细胞们都在玩微信,那外泌体就是他们的“朋友圈”和“私信”,简直是细胞界的“社交达人”!
在我们身体的超级大工厂里,外泌体是个重要的 “快递员” ,它负责在细胞之间传递各种重要信息,对维持我们身体的正常运转,也就是生理平衡,还有疾病的发生发展,都起着关键作用!

外泌体(exosomes)是一种直径约30-150 nm的纳米级囊泡(比头发丝还要细几千倍!),广泛存在于体液中,包括血液、尿液、唾液等。
它们是由细胞内多泡体(multivesicular bodies, MVBs)与细胞膜融合后释放到细胞外的,因此携带了来自亲本细胞的多种生物分子,如蛋白质、脂质、RNA等。这些生物分子不仅反映了亲本细胞的生理状态,还在细胞间通讯中扮演着重要角色。可以说,外泌体是细胞的“心意包裹”,里面装的东西反映了细胞的“心情”和“状态”。
近年来,随着对外泌体研究的深入,科学家们发现不同细胞来源的外泌体具有不同的生物学特性和功能。
图片来自海洛站酷
就像不同的快递员可能会送不同的货,走不同的路线,干不同的活儿一样。例如,免疫细胞和干细胞派出的外泌体,因为它们 “老板”—— 细胞的类型和功能不一样,所以在组成、功能和临床应用上也有很大的差别呢。
免疫细胞外泌体,就像是身体里的“警察快递员”。它们的主要任务是传递“战斗信息”,帮助免疫系统识别和消灭入侵的“坏蛋”,比如病毒、细菌甚至癌细胞。这些外泌体里装的是“战斗指令”和“武器”,比如免疫调节蛋白和抗炎因子,可以说是身体里的“防御特工队”。

而干细胞外泌体,则更像是“建筑工人快递员”。它们的“包裹”里装的是“修复工具”和“建筑材料”,专门负责修复受损的组织,甚至还能促进新细胞的生长。比如,当你受伤时,干细胞外泌体就会带着“修复大礼包”赶到现场,帮助伤口愈合。

今天我们就通过文献汇总,系统的给大家阐述免疫细胞外泌体和干细胞外泌体的差异,以及它们潜在的应用前景。
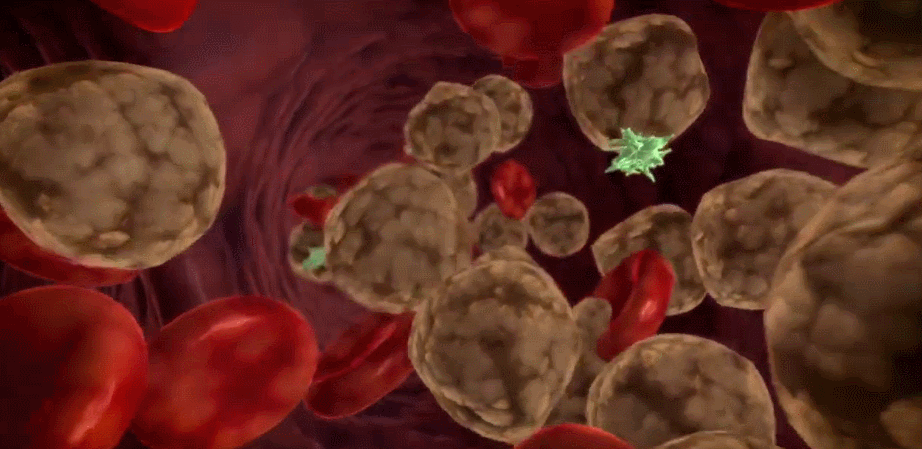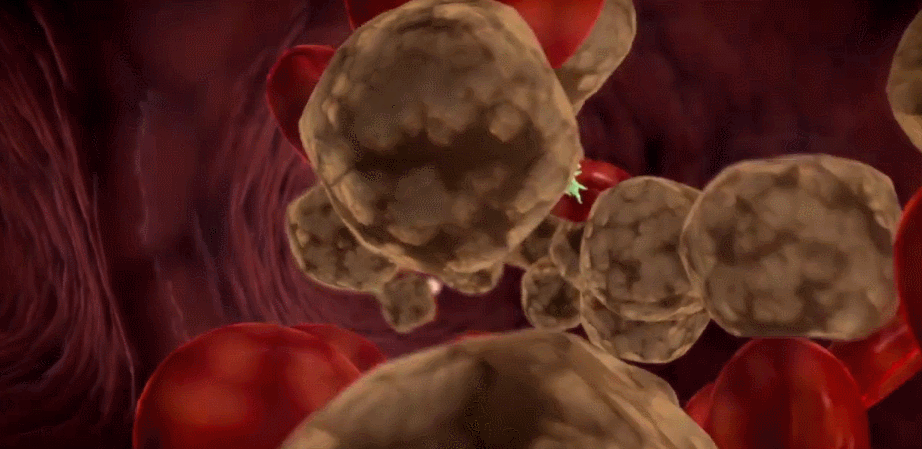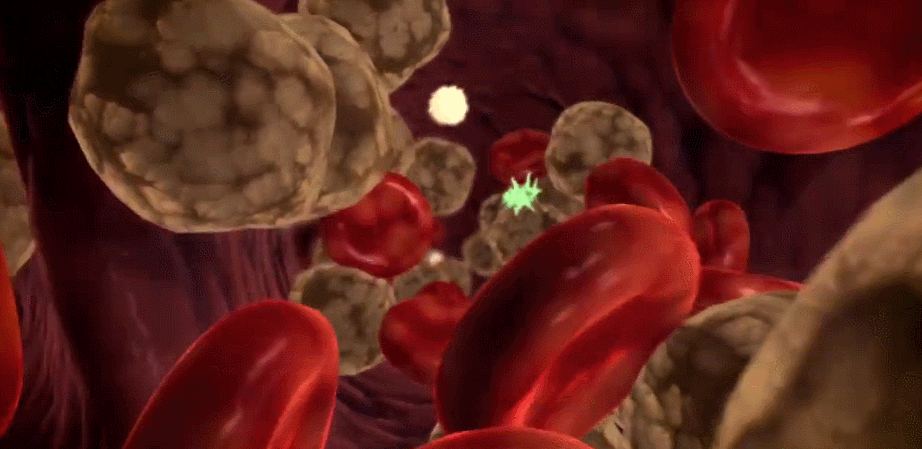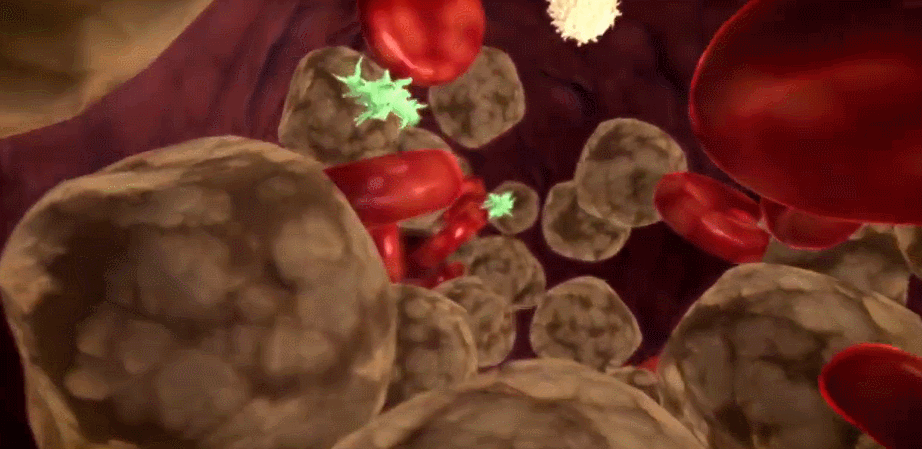
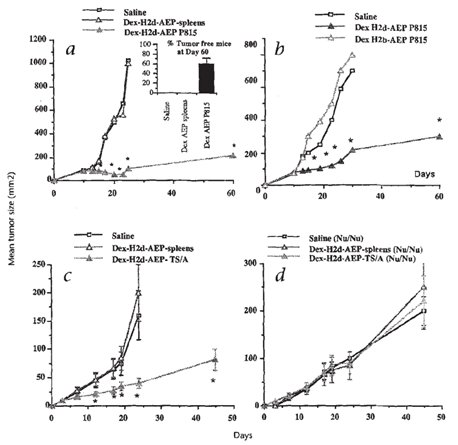
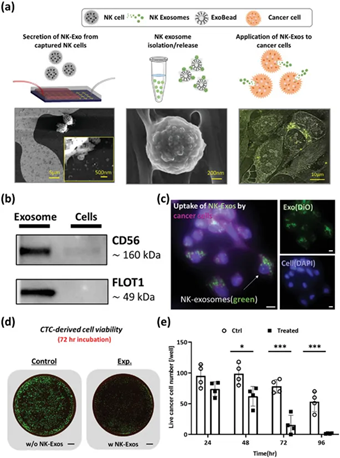
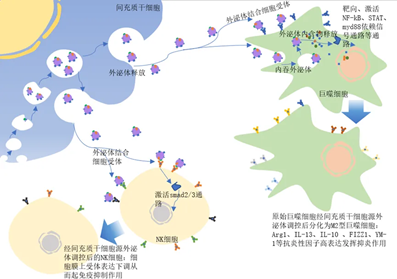
免疫细胞外泌体的特征 免疫细胞,如T细胞、B细胞、树突状细胞(DCs)和巨噬细胞等,分泌的外泌体在免疫应答和调节中发挥重要作用。这些外泌体通常携带母细胞的特定标志物,如MHC分子、共刺激分子和免疫调节分子,能够介导抗原呈递、免疫激活或抑制等过程。 T细胞外泌体:T细胞外泌体富含T细胞受体(TCR)和共刺激分子,如CD3和CD28。这些外泌体可以通过传递TCR信号,激活或抑制其他免疫细胞,从而调节免疫应答。研究表明,T细胞外泌体在自身免疫性疾病和肿瘤免疫逃逸中具有重要作用【1】。 B细胞外泌体:B细胞外泌体携带MHC II类分子和B细胞受体(BCR),能够直接递呈抗原给T细胞,参与体液免疫应答。此外,B细胞外泌体还含有多种microRNAs,如miR-155,这些miRNAs可以调节靶基因的表达,影响免疫细胞的功能【2】。 树突状细胞外泌体:树突状细胞外泌体(Dex)是研究最为广泛的免疫细胞外泌体之一。Dex携带MHC I类和II类分子、共刺激分子(如CD80和CD86)以及多种免疫调节分子,能够有效激活T细胞和B细胞,诱导特异性免疫应答。Dex在肿瘤免疫治疗中显示出巨大的潜力【3】。 骨髓来源树突状细胞(BM-DCs)外泌体给药后的抗肿瘤效果。图片引用自文献3 巨噬细胞外泌体:巨噬细胞外泌体富含炎症相关分子,如TNF-α、IL-1β和IL-6。这些外泌体在炎症反应和感染中发挥重要作用。例如,M1型巨噬细胞外泌体可以通过传递炎症因子通常促进炎症,而M2型则具有抗炎和组织修复功能,从而影响疾病进程【4】。 NK细胞外泌体:NK细胞释放的细胞外囊泡在肿瘤治疗领域十分具有前景,其携带的具有抗肿瘤作用的蛋白质和microRNAs,有望成为一种有前景的新抗癌方法【9】。基础实验发现,NK细胞外泌体可以刺激免疫细胞;此外,其还可减轻肿瘤细胞的免疫抑制效应,这可能与其可降低T细胞表明程序性死亡受体(PD-1)的表达等有关【10】。 例如一项研究发现,在一小群非小细胞肺癌 (NSCLC) 患者中,分离了NK 细胞及其外泌体以及循环肿瘤细胞 (CTC),结果与健康供体相比,NSCLC患者具有大量 NK 和 NK 外泌体;研究进一步证明,采集的 NK细胞外泌体对 CTC 表现出细胞毒性作用。 图片引用自文献10 干细胞外泌体的特征 干细胞,包括间充质干细胞(MSCs)、胚胎干细胞(ESCs)和诱导多能干细胞(iPSCs)等,分泌的外泌体在组织修复和再生中具有重要作用。这些外泌体通常富含生长因子、细胞因子和调节性miRNA,能够促进细胞增殖、抑制凋亡和调节免疫反应。 间充质干细胞外泌体(MSC-exo):研究发现,间充质干细胞分泌外泌体的能力最强,是目前研究最为广泛的干细胞外泌体【11】。MSC-exo富含多种生长因子、细胞因子和miRNAs,如VEGF、HGF和miR-21。 图片引用自文献11 这些外泌体通过促进血管生成、抑制炎症和纤维化,参与组织修复和再生。MSC-exo在多种疾病模型中显示出治疗效果,如心肌梗死、肝纤维化和神经退行性疾病【5】。 免疫细胞外泌体与干细胞外泌体的对比 免疫细胞和干细胞均可分泌外泌体参与机体生理过程,然而成分组成的差异性决定了两者在功能上的不同侧重点以及应用差异。它们在以下几个方面表现出明显的差异性: 外泌体组成与功能差异表 随着对外泌体研究的深入,越来越多的证据表明,不同细胞类型来源的外泌体具有独特的生物学特性和功能。未来,基于外泌体的治疗策略将更加个性化和精准化。例如,通过工程化改造外泌体,可以增强其靶向性和治疗效果;通过联合应用不同细胞类型的外泌体,可以实现协同治疗。 此外,外泌体作为生物标志物的潜力也备受关注。通过分析体液中特定细胞类型的外泌体,可以实现疾病的早期诊断和预后评估。例如,肿瘤细胞外泌体携带的突变基因和miRNAs可以作为肿瘤诊断的标志物【8】。
小结
免疫细胞和干细胞外泌体在组成、功能和应用上存在显著差异。免疫细胞外泌体主要参与免疫调节和抗原呈递,而干细胞外泌体则侧重于组织修复和再生。随着研究的深入,基于外泌体的治疗策略和诊断工具将为多种疾病的治疗和管理提供新的思路和方法。这两类外泌体在精准医学、联合治疗和药物递送等领域的应用前景将更加广阔。未来的研究应进一步揭示外泌体的生物学机制,并探索其临床应用潜力,为人类健康事业做出更大贡献。
1. Thery, C., et al. (2002). Exosomes: composition, biogenesis and function. *Nature Reviews Immunology*, 2(8), 569-579.
2. Robbins, P. D., & Morelli, A. E. (2014). Regulation of immune responses by extracellular vesicles. *Nature Reviews Immunology*, 14(3), 195-208.
3. Zitvogel, L., et al. (1998). Eradication of established murine tumors using a novel cell-free vaccine: dendritic cell-derived exosomes. *Nature Medicine*, 4(5), 594-600.
4. Zhang, B., et al. (2015). Macrophage-derived exosomes in cancers: biogenesis, functions and therapeutic applications. *Oncotarget*, 6(30), 28841-28856.
5. Lai, R. C., et al. (2010). Exosome secreted by MSC reduces myocardial ischemia/reperfusion injury. *Stem Cell Research*, 4(3), 214-222.
6. Ratajczak, M. Z., et al. (2006). Embryonic stem cell-derived microvesicles reprogram hematopoietic progenitors: evidence for horizontal transfer of mRNA and protein delivery. *Leukemia*, 20(5), 847-856.
7. Zhu, W., et al. (2017). Exosomes derived from human pluripotent stem cells promote tissue regeneration in a chemically induced liver fibrosis model. *Stem Cells International*, 2017.
8. Melo, S. A., Luecke, L. B., Kahlert, C., Fernandez, A. F., Gammon, S. T., Kaye, J., ... & Kalluri, R. (2015). Glypican-1 identifies cancer exosomes and detects early pancreatic cancer. *Nature*, 523(7559), 177-182.
9.Fabbri M. Natural Killer Cell-Derived Vesicular miRNAs: A New Anticancer Approach?. Cancer Res. 2020;80(1):17-22.
10.Han D, Wang K, Zhang T, Gao GC, Xu H. Natural killer cell-derived exosome-entrapped paclitaxel can enhance its anti-tumor effect. Eur Rev Med Pharmacol Sci. 2020;24(10):5703-5713.
11.郭嘉,丁琼桦,刘泽,等.间充质干细胞来源外泌体的生物学特性及免疫调控作用[J].中国组织工程研究, 2022, 26(7):9.
相关新闻
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
