




引言
今日分享新的案例文献:研究发现,胎盘来源间充质干细胞在缺血组织再生、免疫调节和血管生成等方面具有独特的特性,因此其治疗效益有潜力用于重度肢体缺血患者(CLI)的临床治疗。在一项I期临床试验中,9名CLI患者在接受2000万至6000万个胎盘间充质干细胞后,休息时疼痛症状、溃疡愈合方面和最大步行距离均有显著改善。
重症肢体缺血(CLI):亟需治疗新方案
随着现代生活节奏的不断加快,越来越多的压力朝“996模式”,甚至“007模式”的“上班族”们涌来,与压力同时接踵而来的还有久坐不动,暴饮暴食等不健康的方式。而这恰恰也成为了重度肢体缺血(CLI)的重要病因之一,CLI是外周动脉病变的一种,常表现为肢体疼痛,未予诊治还有可能导致患者截肢的情况,是一种不容忽视的疾病。目前,血管内血运重建术或开放手术是目前治疗这类疾病的标准治疗方法。然而,由于内部血管解剖不充分或手术风险高,20-40%的个体不适合这些治疗。
胎盘间充质干细胞:有前景的CLI新疗法
最近,发表在“Stem Cell Research & Therapy”上的新临床试验揭示了胎盘来源的间充质干细胞(P-MSCs)可作为治疗CLI的一种新疗法且具有巨大的临床前景[1]。

科学研究发现,由于胎盘来源间充质干细胞在缺血组织再生和通过免疫调节和血管生成恢复组织功能方面的独特特性,胎盘来源间充质干细胞的治疗效益可以被用于CLI受试者。
这项I期试验研究的对象为9名CLI患者,这些患者按剂量被分为两个组,分别注射20× 10*6和60× 10*6的P -MSCs细胞,方法为往肌肉注射两次,两次注射间隔两个月。在术后的随访中,我们发现,当CLI患者注入P-MSC后,患者休息时疼痛症状、溃疡愈合方面和最大步行距离均有显著改善。
研究人员将分离和体外扩增后的胎盘来源间充质干细胞注射到缺血肢体,胎盘来源间充质干细胞通过分泌免疫调节细胞因子抑制炎症,促进免疫调节,刺激M2巨噬细胞的诱导,增加循环调节性T细胞的数量,导致白细胞介素IL-10的增加和炎症的消退。此外,间充质干细胞释放的因子还直接促进血管生成。具体作用示意图如下图所示。
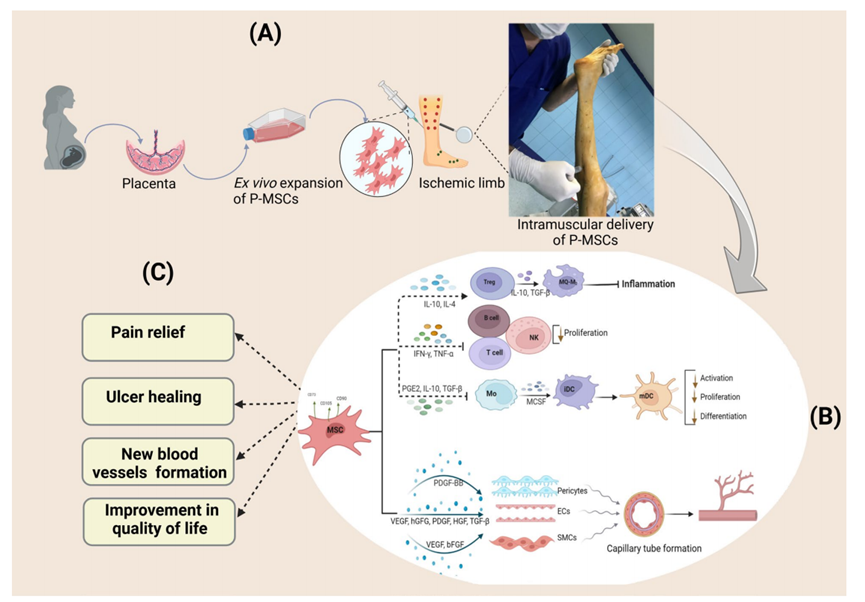
(图片来自参考文献1)
研究还动态观察将胎盘源性间充质干细胞植入6个月后血管造影的动态示意图,造影显示侧支动脉在给予P-MSC 6个月后有明显的增加。
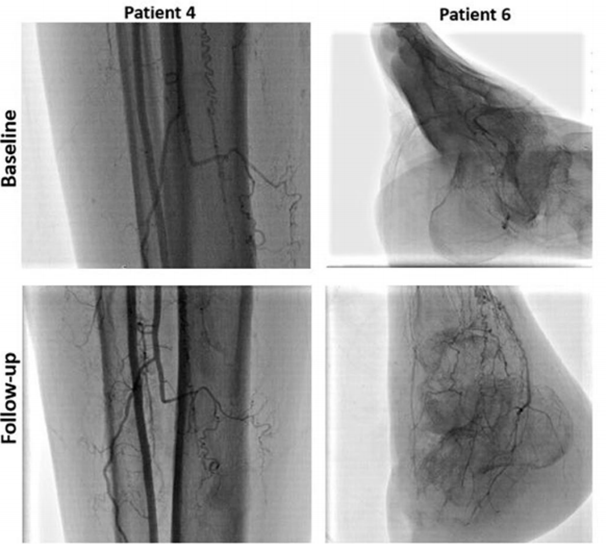
(图片来自参考文献1)
在6个月的随访中,患者缺血性溃疡/坏疽的肢体也呈现明显愈合。整个溃疡表面测量大大减少,坏疽没有进展。
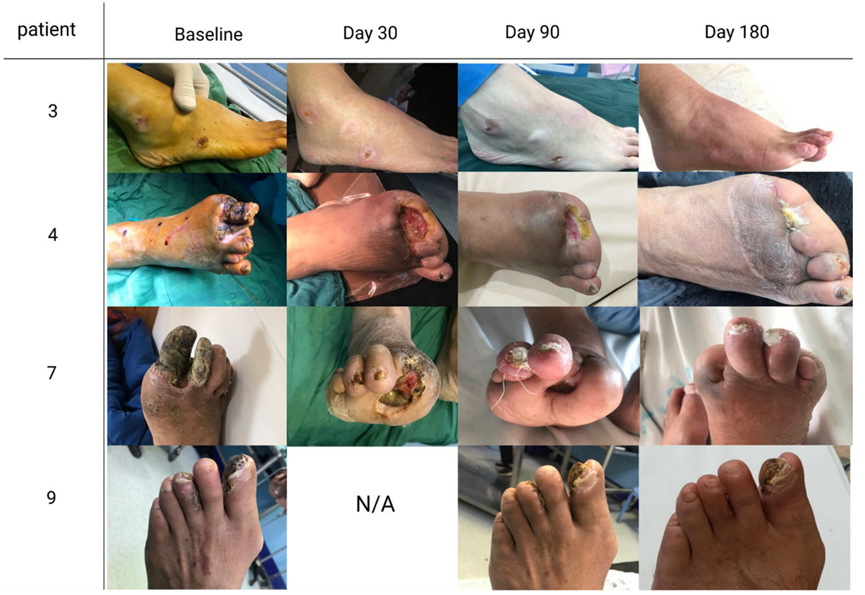
(图片来自参考文献1)
这无疑对于CLI的临床治疗描绘了新的治疗诗篇,那么接下来就让我们一起走进CLI与P-MSCs的世界。
CLI:不容小觑的“截肢杀手“
重度肢体缺血是PAD最严重的形式,可导致缺血性休息痛、未愈合的伤口、坏疽和肢体截肢。血管内血运重建术或开放手术是目前改善患肢血流的标准治疗方法。然而,由于内部血管解剖不充分或手术风险高,20-40%的个体不适合这些治疗。
此外,美国食品和药物管理局(FDA)还没有批准治疗CLI患者的药物,目前只能通过伤口护理、疼痛控制来控制疾病的并发症。最终,对于那些没有其他选择、不适合手术的人来说,截肢有时是最后的手段。据估计,这些患者的死亡率为30%,截肢风险为40%。[2]鉴于治疗限制和高死亡率,CLI患者的生活质量与晚期癌症患者的生活质量相当。
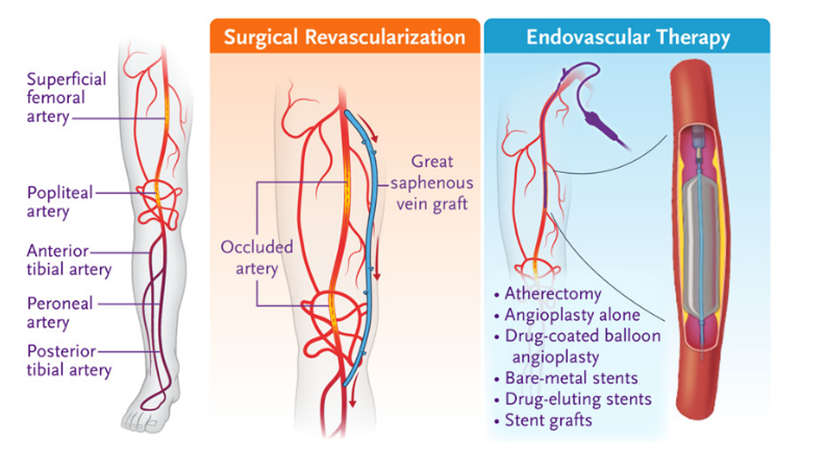
(图片来自参考文献2)
胎盘间充质干细胞:CLI临床修复机制
在简单了解完CLI的临床表现以及相应预后之后,我们可以知道目前对于CLI的临床治疗方案还非常有限,而近些年间随着干细胞疗法的进一步发展和研究,干细胞疗法为CLI的诊治提供了新的临床诊疗思路。
间充质干细胞(Mesenchymal stem cells, MSCs)因其独特的生物学特性而被视为重度肢体缺血的再生疗法。研究表明,胎盘来源的间充质干细胞(P-MSCs)表现出与胎盘血管生态位中检测到的其他间充质干细胞几乎相同的形态学特征[3]。下图所示为各种类型的P-MSCs。
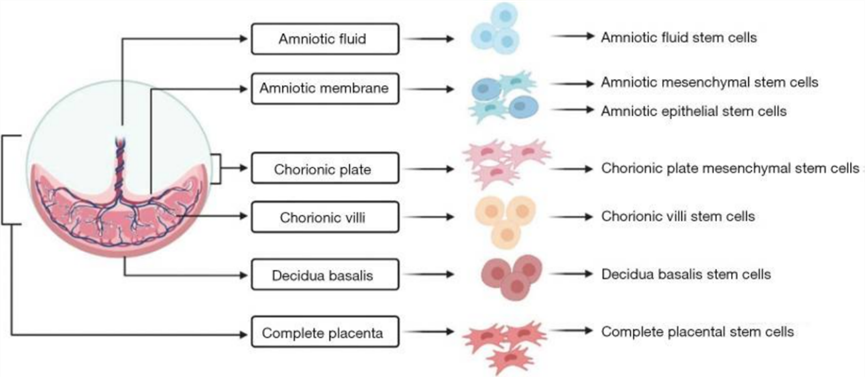
(图片来自参考文献3)
P-MSCs在多项临床研究试验中已展现其治疗的强大潜力,其治疗作用机制可大致为以下两点。
机制一:增加“外援“
根据上述的阐述,CLI的发生是因为机体的灌注不足,造成机体四肢的血供不足从而造成一系列临床症状的发生。而据研究发现P-MSCs可以显著增加微血管密度,增加“外援”,增加了损伤部位的血液灌注,并消除了疾病的症状。
如下图所示,在P-MSC的作用下,毛细血管网有明显的增多,P-MSCs在血管生成程度上还可以与其他细胞合作,并具有分化为内皮细胞和平滑肌血管细胞的能力,以增加缺血器官的血管生成[4]。
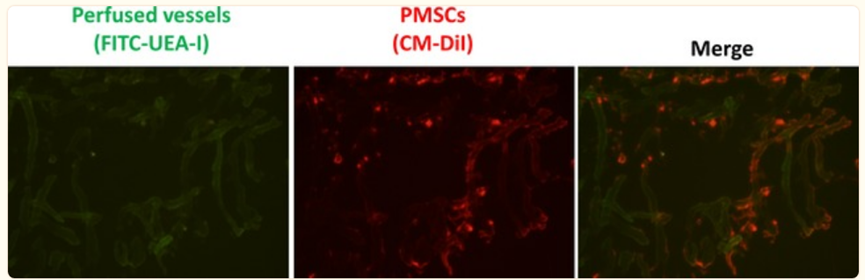
(图片来自参考文献4)
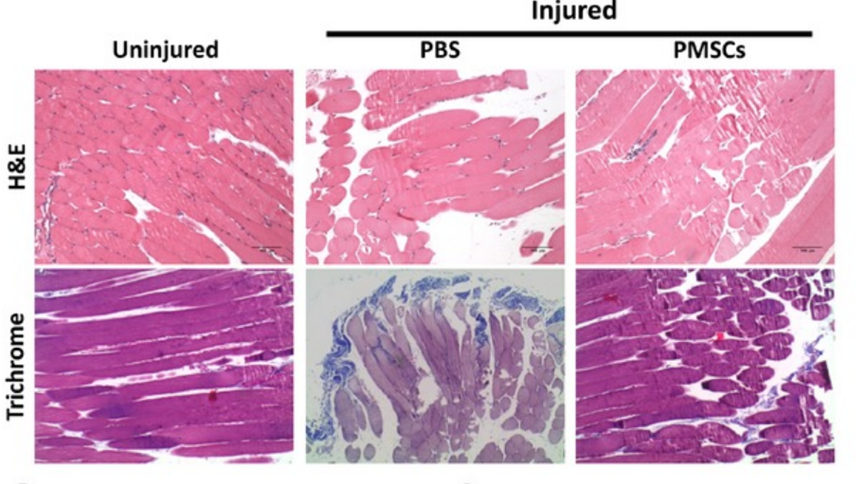
(图片来自参考文献4)
机制二:“同化自身,增强友军buff“
干细胞疗法有一个主要的问题是发生免疫排斥的几率很高,但P-MSCs可表现出有限水平的HLA-A、HLA-B和HLA-C分子,这可以在很大程度上降低免疫原性,使“自身同化“,不会让自身免疫细胞”误击“到,增加了P-MSCs的移植适应性,使得P-MSCs疗法具有可行性。
其次,P-MSCs可使发挥促炎作用的M1细胞转化为发挥抗炎作用的M2细胞。He等研究表明[5],将胎盘间充质细胞(PDA-002)注射到CLI小鼠模型中,可增加缺血组织中M2抗炎巨噬细胞。
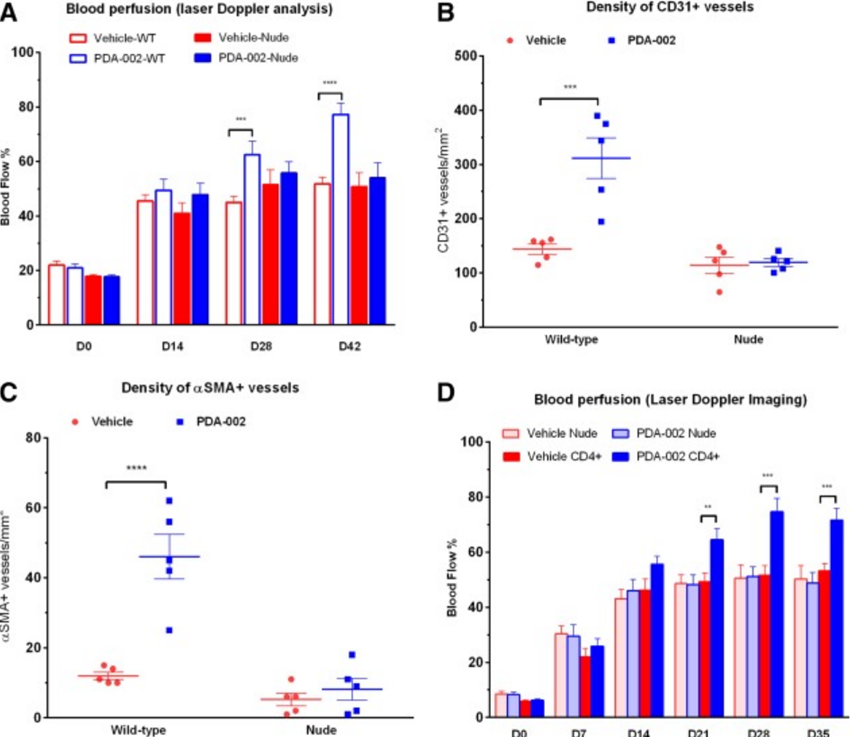
(图片来自参考文献5,PDA-002为人胎盘来源的MSC样细胞)
小结
随着近些年来越来越多临床试验的开展,间充质干细胞在缺血性疾病治疗方面展现了巨大的潜力,从这项早期临床试验中可以观察到,用高剂量的胎盘来源间充质干细胞进行肌肉注射治疗是安全且耐受性良好的。这对于CLI等缺血性疾病的临床治疗可以提供借鉴意义,然而,为了填补关于间充质干细胞治疗严重肢体缺血特性的知识空白,还需要进行更多的大型随机临床试验,但我们相信,间充质干细胞疗法在未来定会为临床诊治这类疾病时提供又一选择!
参考文献:
[1] Shirbaghaee Z, Heidari Keshel S, Rasouli M, Valizadeh M, Hashemi Nazari SS, Hassani M, Soleimani M. Report of a phase 1 clinical trial for safety assessment of human placental mesenchymal stem cells therapy in patients with critical limb ischemia (CLI). Stem Cell Res Ther. 2023 Jul 5;14(1):174. doi: 10.1186/s13287-023-03390-9. PMID: 37408043; PMCID: PMC10324209.
链接:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10324209/
[2] Farber, Alik et al. “Surgery or Endovascular Therapy for Chronic Limb-Threatening Ischemia.” The New England journal of medicine vol. 387,25 (2022): 2305-2316. doi:10.1056/NEJMoa2207899
链接:
https://www.nejm.org/doi/10.1056/NEJMoa2207899?url_ver=Z39.882003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
[3] Siddesh SE, Gowda DM, Jain R, Gulati A, Patil GS, Anudeep TC, Jeyaraman N, Muthu S, Jeyaraman M. Placenta-derived mesenchymal stem cells (P-MSCs) for COVID-19 pneumonia-a regenerative dogma. Stem Cell Investig. 2021 Feb 3;8:3. doi: 10.21037/sci-2020-034. PMID: 33688491; PMCID: PMC7937692.
链接:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7937692/
[4] Xie N, Li Z, Adesanya TM, Guo W, Liu Y, Fu M, Kilic A, Tan T, Zhu H, Xie X. Transplantation of placenta-derived mesenchymal stem cells enhances angiogenesis after ischemic limb injury in mice. J Cell Mol Med. 2016 Jan;20(1):29-37. doi: 10.1111/jcmm.12489. Epub 2015 Aug 18. PMID: 26282458; PMCID: PMC4717860.
链接:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4717860/
[5] Shuyang He, Joseph Gleason, Ewa Fik-Rymarkiewicz, Andrea DiFiglia, Mini Bharathan, Andrew Morschauser, Ivana Djuretic, Yan Xu, Michael Krakovsky, Vladimir Jankovic, Charito Buensuceso, James Edinger, Uri Herzberg, Wolfgang Hofgartner, Robert Hariri, Human Placenta-Derived Mesenchymal Stromal-Like Cells Enhance Angiogenesis via T Cell-Dependent Reprogramming of Macrophage Differentiation, Stem Cells, Volume 35, Issue 6, June 2017, Pages 1603–1613
链接:https://doi.org/10.1002/stem.2598
相关新闻
博雅新闻

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
