




免疫细胞治疗已然成为医学发展的焦点。近年来,免疫细胞治疗恶性肿瘤在全球各国逐渐扩大应用,并形成了一些专家共识及实践建议。免疫细胞治疗的问世,让人类“攻克”恶性肿瘤又向前迈进了一步。日前,science杂志上刊登了一则综述,总结了用免疫细胞治疗人类疾病所取得的进展,以及工程化免疫细胞的新兴策略、该领域面临的挑战,特别强调迄今为止应用最多的癌症治疗。

工程化免疫细胞疗法是人为将免疫细胞进行改造,以便输入患者体内时,识别和响应疾病状态,又被称为“活着的药物”。工程化免疫细胞疗法已进入临床应用,多种工程化T细胞疗法被批准用于治疗血液系统恶性肿瘤。众多研究者正在进行临床前和临床研究以改变免疫细胞的命运和功能,将其广泛应用于癌症、传染病等。
免疫细胞治疗的发展历程
免疫细胞疗法(ICT)首次出现在80年代末,从癌症病人中分离出的肿瘤浸润T细胞被用于治疗转移性黑色素瘤,这些早期临床试验的结果,推动了ICT的探索和发展,并将ICT应用于传染病和自身免疫等。然而,T细胞免疫疗法还面临着大量挑战,如在许多类型的癌症中,分离和制备大量具有功能的肿瘤特异性T细胞较为困难等。
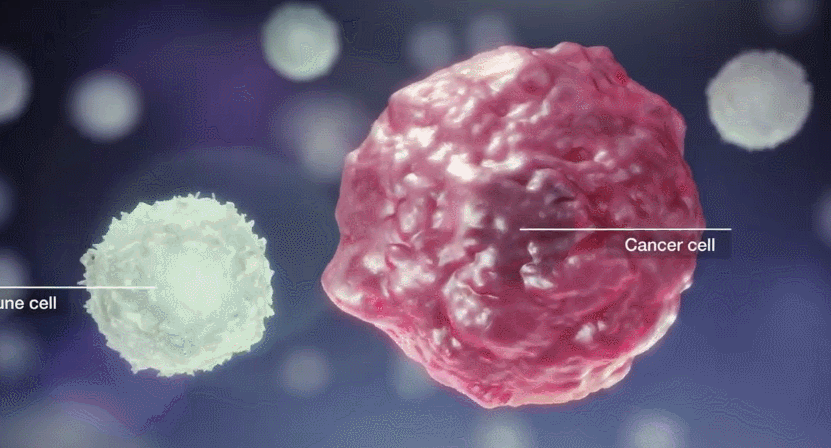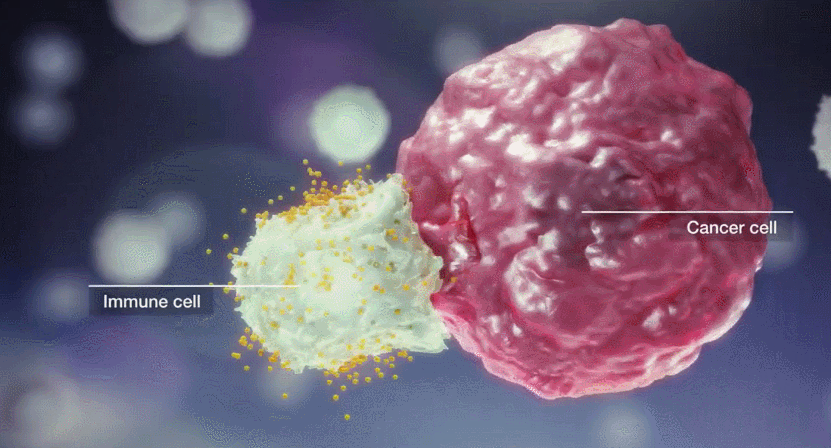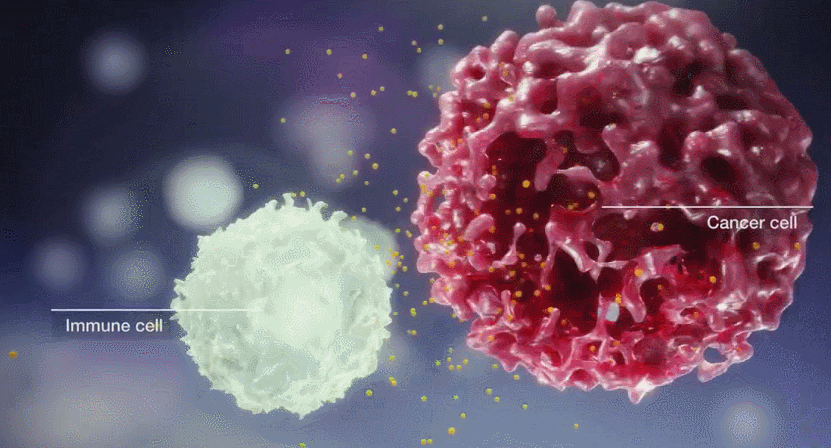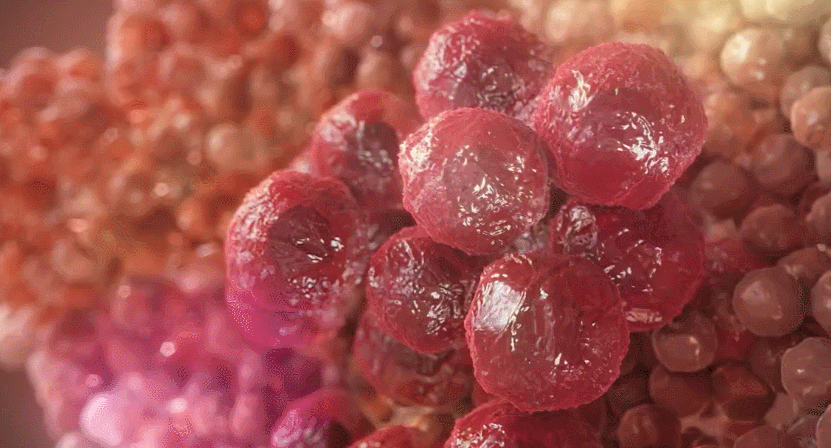
工程化免疫细胞的方法包括药理操作和基因修饰等多种技术。它们可以在细胞治疗输注前于体外进行,也可以直接在体内进行。基因工程在临床上ICT的发展中发挥了关键作用,有几个重要的修改类别:
(i)抗原受体工程化:包括转基因T细胞受体(TCRs)和嵌合抗原受体(CARs);
(ii)调节代谢、存活和增殖等自然特性的基因回路;
(iii)引入辅助基因,为免疫细胞提供新功能;
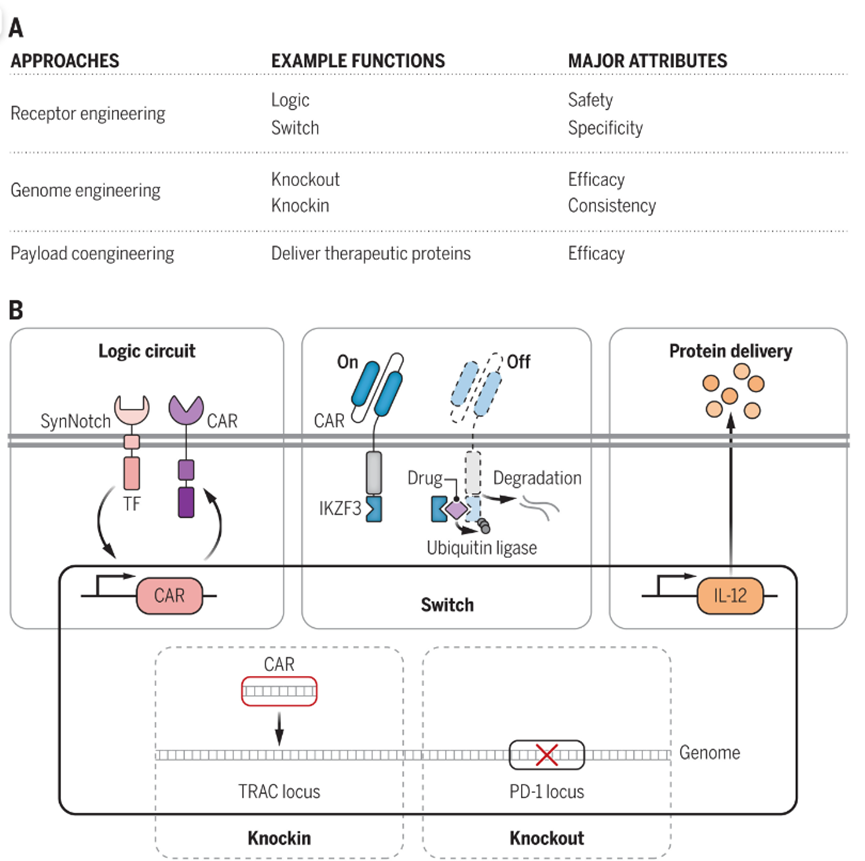
[1]体外免疫细胞工程
第一个FDA批准的免疫细胞治疗产品是以细胞为基础的癌症疫苗Provenge,该疗法于2010年在美国获得批准。
在过去的5年中,6种用于血液系统恶性肿瘤的CAR-T细胞疗法和一种用于治疗先天性无胸腺症免疫缺陷的工程胸腺组织疗法已在美国获得批准。
此外,包含肿瘤浸润淋巴细胞的ICT以及用于表达明确T细胞受体的T细胞疗法获批在即,以及数千项针对不同疾病的免疫细胞疗法的临床试验也在紧锣密鼓进行中。这些都预示着免疫细胞治疗庞大的临床应用前景。
CAR-T免疫细胞疗法的临床进展
2017年,第一个获批的“细胞和基因疗法”是一种靶向CD19的CAR-T细胞疗法。CAR 的表达使T细胞以一种不依赖MHC的方式,实现对目标抗原的特异性识别,并有效地启动细胞的细胞毒性,诱导其产生细胞因子并进行扩增,在某些情况下,还启动长期记忆形成。
第一代CAR结构域单一,临床疗效有限,第二代CAR加入CD28或4-1BB的共刺激信号结构域,靶向CD19抗原,早期试验显示对B细胞淋巴瘤和白血病有效。此后十年,靶向CD19的CAR-T细胞的临床开发进展迅速,FDA批准了4种不同CD19靶向的CAR-T细胞产物用于B细胞恶性肿瘤,早期临床研究提示这些产物对难治性或复发性疾病患者存在良好疗效,可与标准高剂量化疗相比。

图片来自文献[1]
此外,两种靶向B细胞成熟抗原(BCMA)的CAR-T细胞产品已在多发性骨髓瘤中进行测试并且获得批准,且在病人中响应良好。
与此同时,基于转基因的T细胞受体(TCR-T cells)的ICT也在研究中。与CAR-T细胞相比,TCR-T细胞可以识别源自突变或过表达的细胞内蛋白的肽,从而扩大了潜在抗原靶标的空间。TCR-T试验还处于早期阶段,但已经看到了有希望的客观缓解率。
CAR-T免疫细胞治疗癌症之外的疾病
T细胞疗法已被用于癌症以外的疾病的临床试验,如自身免疫、移植耐受和移植物抗宿主病,尽管其中许多研究还处于非常早期的阶段:用CD19 CAR-T细胞产物治疗难治性狼疮患者,发现患者全身自身抗体水平迅速下降和疾病缓解;
当前正在进行的CAR-T识别I类MHC分子人白细胞抗原HLA-A2,抑制HLA-A2肾脏和肝脏移植的排斥反应临床试验;
在HIV中,测试了以HIV-1中和抗体作为结合域产生的CAR,被证明是安全的,且在患者暂时暂停抗逆转录病毒治疗后延迟病毒反弹长达10周,并暂时减少了病毒库。此外,基于其他免疫细胞的疗法现在也进入临床试验中。
现在有数百家机构正在开发新型工程化T细胞,使用CAR,TCR和各种新的合成抗原受体,以及增强T细胞功能的其他功能。目前,clinicaltrials.gov上列出的“CAR-T细胞”的临床试验超过1000项。
免疫细胞治疗的发展策略一:体外细胞工程
受到生物网络复杂性的启发,研究人员设计了复杂的工程免疫细胞,使其能够感知和响应不同的刺激组合,并增强其疗效。从临床角度来看,治疗性免疫细胞设计有三个主要目标:提高靶点特异性、有效性和安全性。监管、制造和商业(例如成本)挑战也开始影响细胞疗法。从离体工程的角度来看,临床细胞设计目标通常通过三种基因和分子工程方法实现,包括受体工程、宿主细胞基因组工程和治疗有效载荷协同工程。
抗原受体工程:对免疫细胞表面受体进行修饰和蛋白质工程,以提高靶向特异性和安全性,最典型的就是CARs。CARs结合了TCR和共刺激受体信号结构域,控制T细胞增殖、效应功能和代谢适应性,明确靶向、杀伤特定癌细胞。与TCR相比,CAR能够靶向任何表面抗原,但抗原敏感性低。基于此,研究者开展了混合型受体设计:结合CAR和TCR的优势的TruCs(T细胞受体融合结构)、STARs[合成TCR和抗原受体]和HIT[HLA非依赖性TCR],这些新受体显示出明显的体内活性和抗原敏感性。

治疗有效载荷协同工程:除了表达抗原特异性受体外,改变工程化免疫细胞表达的治疗性有效载荷,还为调节细胞功能提供了附加维度。当与CAR表达相结合时,它们有时被称为“装甲”CAR或TRUCK(T细胞重定向到普遍细胞因子杀伤)。一些最有希望的治疗有效载荷是分泌因子,如细胞因子、治疗性抗体或重塑肿瘤微环境,激活药物前体的酶。当前正在开展的研究有:设计表达IL-15的NK细胞,IL-15是NK细胞存活的关键细胞因子;转导表达IL-12的骨髓细胞以对抗实体瘤中发现的免疫抑制基因标记。
基因组工程:除了肿瘤特异性受体和免疫调节因子的表达外,最近的工作已证明改造免疫细胞基因组工程提高细胞治疗有效性和安全性。此外,如果免疫细胞来源是同种异体的,基因组工程还可以降低细胞疗法输入后可能会引起的排斥反应风险。此外,已经对免疫细胞进行了许多敲除筛选以鉴定基因,我们现在正在等待,看看哪一种在临床上影响最大。在最近一项针对八名患者的临床试验中,使用CRISPR-Cas将CD19 CAR整合到PD-1位点的T细胞在一些患者中显示出87%的完全缓解率,并且没有免疫效应细胞相关的神经毒性综合征。
免疫细胞治疗发展策略二:体内细胞工程
在过继转移后,工程化免疫细胞在寻找和破坏其靶标方面面临许多挑战,包括存活足够的时间,归巢到适当的部位并吸引靶细胞,以及维持适当的表型以清除癌症等。为克服上述困难,研究者发展了一系列技,包括开发将免疫细胞递送至指定位点的材料,用外界可控的线索来指示转移的细胞,以及直接对生物体进行遗传操纵。
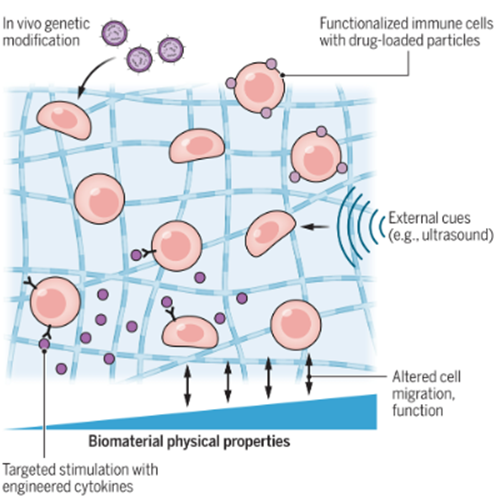
[1] 体内免疫细胞工程手段
靶向刺激转移细胞:通过对转移的细胞提供有针对性的体内刺激的策略,实现治疗效果和安全性的适当平衡。例如,FDA批准的小分子药物具有良好的生物利用度和药代动力学,因此已被用于控制基因开关,实现对工程化T细胞功能的快速、可逆的动态调节。这将允许我们严格控制CAR-T细胞治疗的活性,同时减少临床前研究中T细胞的耗竭,并且还提供了安全开关,允许在毒性发作时关闭细胞活性。例如,将细胞因子包装成纳米颗粒和微粒,这些纳米颗粒和微粒可以在转移前粘附到免疫细胞上,或通过代谢标记靶向体内免疫细胞,以使细胞因子活性定位到所需的治疗部位,具有最小的全身暴露,减轻副作用。
调节免疫细胞的工程化系统:生物材料策略提供了另一个提高 ICT 有效性的机会,该策略允许我们直接在体内操纵免疫细胞,并且可以与宿主免疫和过继细胞治疗进行协同应用。生物材料可以在恶劣的环境中保护分子和细胞货物,将治疗定位到所需的解剖位置,并控制宿主细胞的运输和活化。如通过一定的载体将T细胞、抗原呈递细胞等输送到所需位置病保持理想表型,发挥其细胞功能。
体内直接基因修饰:在转移前对培养的细胞进行工程化改造不仅过程复杂、造价昂贵,且耗时长。这些限制因素促使人们探索原位基因修饰宿主细胞的方法,来绕过体外操作的阻碍。CAR编码逆转录病毒颗粒已被整合到用于转移人类免疫细胞的植入式支架中,从而在体内生成CAR-T细胞。动物实验证实这一方法有效。
小结:总的来说,工程化免疫细胞用于治疗已经取得了非常大的进步,但寻找更安全、更有效的免疫细胞治疗方法仍存在巨大的探索空间。工程化免疫细胞的高昂成本和复杂制造过程,是免疫细胞疗法在医学上的长期应用所面临的两个关键挑战。为了使工程化免疫细胞疗法充分发挥其潜力,未来仍然需要多样化的科学努力。
参考文献:
[1] Irvine DJ, Maus MV, Mooney DJ, Wong WW. The future of engineered immune cell therapies. Science. 2022;378(6622):853-858. doi:10.1126/science.abq6990
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
