




近日,发表在《World journal of stem cells》上的一篇综述[1],概述了干细胞疗法在肾脏疾病中的应用及其最新进展,指出干细胞疗法在肾脏疾病再生医学领域具有巨大潜力。

据世界卫生组织(WHO)估计,全世界每年有多达 1000 万人死于肾脏疾病,到 2040 年,慢性肾病(CKD)预计将成为全球第五大死因。目前肾脏疾病的常规治疗是药物,但这些药物只能延缓疾病进展,不能逆转病情的发展。研究表明,干细胞疗法具有治疗肾脏疾病的作用,可减轻肾脏损伤,同时改善肾小球和肾小管的功能和结构,有望治愈、逆转或减轻肾脏疾病。
No.1
不同类型干细胞治疗肾脏疾病
近年来,包括胚胎干细胞、内皮祖细胞、间充质干细胞等不同类型的干细胞均被应用到了肾脏疾病的治疗研究当中。
胚胎干细胞(ESC)是具有无限分化潜能的多能细胞。研究表明,将胚胎干细胞直接植入小鼠胚胎肾培养物可产生胚胎干细胞衍生的肾小管和近端肾小管细胞。将胚胎干细胞暴露于特定的诱导剂或因子也会使得细胞在体外分化成肾系细胞。但是,胚胎干细胞衍生的分化细胞本质上是同种异体的,可以表达特定的表面蛋白来触发受体的免疫系统。因此,如果同种异体移植物未能与受体实现免疫相容性,则可能会出现急性和慢性排斥反应或移植物抗宿主病。

图1(来自文献[1]):肾脏及其主要成分。A:肾;B:肾单位的放大倍数;C:肾小体;D:肾小球。足细胞、系膜细胞和毛细血管内皮细胞是肾小球结构的一部分。
第二类是内皮祖细胞(EPC)。内皮祖细胞在维持血管完整性和修复任何形式的内皮损伤方面具有重要作用。内皮祖细胞可以从不同的细胞来源中分离出来。内皮祖细胞疗法的有益效果已在急性肾损伤、慢性肾病和肾动脉狭窄等动物模型中得到研究证实。
在干细胞治疗肾脏疾病的治疗研究中,最常用的是间充质干细胞。
多年来,研究人员发现间充质干细胞(MSCs)可以从各种器官或组织中分离出来,如脂肪组织、脐带、胎盘、外周血、羊水和骨骼肌。间充质干细胞是激活受损肾脏再生的最有效的细胞群类型之一,大量研究表明,间充质干细胞既可以分化为一般的肾细胞[4] ,也可以特异性分化为肾成分细胞,如肾上皮细胞、系膜细胞和内皮细胞。

临床前研究已证明间充质干细胞在急性肾损伤和慢性肾病动物模型中的治疗潜力[5]。根据对 70 多篇文章的系统评价证实:间充质干细胞是治疗实验性慢性肾病最有效的细胞群之一[4]。同时,在一项涉及慢性和急性肾损伤动物模型的荟萃分析中,尽管给药方式不同(动脉、静脉或肾脏),间充质干细胞仍能使得肾脏再生[5]。
No.2
干细胞治疗肾脏疾病的临床转化
许多动物实验证明了干细胞疗法对肾脏疾病的有效性,然而由于动物模型和人体生理学的不同,干细胞治疗肾脏疾病的临床转化仍然需要一定的时间。
截至 2021 年 3 月,美国国家医学图书馆注册了 40 多项正在进行或已完成干细胞治疗肾脏疾病相关的临床试验,大多数使用的是间充质干细胞。


表格1(来自文献[1]):基于间充质干细胞和内皮祖细胞的肾脏疾病治疗临床试验
在这些试验中,有使用来自不同组织来源(骨髓、脂肪、脐带等)的间充质干细胞。在其中的一项研究中,患有术后急性肾损伤高风险并接受心脏手术的患者接受了同种异体骨髓来源的间充质干细胞(BM-MSC),患者在施用间充质干细胞后没有出现副作用,间充质干细胞还保护患者免受术后早期和晚期肾功能恶化[6]。
同时,目前已经进行了多个间充质干细胞治疗慢性肾病的人体试验。根据一项评估自体脂肪间充质干细胞(AD-MSCs)治疗慢性肾病的安全性和临床可行性的初步研究报告所述,这些细胞疗法是安全的并且没有产生任何不良反应[8]。

这些数据表明,移植间充质干细胞是安全的、耐受性良好的,并且在免疫抑制方案的基础上,间充质干细胞可以发挥增强抑制肾移植后宿主免疫反应的作用。不过,也有一些研究得出不一致的结论,因此未来仍然需要开展更多的研究来探讨间充质干细胞治疗不同肾脏患者的疗效。
No.3
展望:干细胞治疗仍需突破
干细胞已经被广泛应用到多系统疾病的治疗研究当中。在肾脏疾病领域,临床前以及现有的一些临床研究数据均显示了干细胞治疗的安全性和有效性。然而,干细胞治疗肾脏疾病的临床转化仍然需要克服许多障碍,例如对肾脏疾病的副作用仍需进一步研究,现有的初步结果仍缺乏长期随访数据等等。
而事实上,针对其他疾病的干细胞疗法在临床转化时也同样面临类似的问题。不过,随着干细胞临床试验在全球如火如荼的开展,干细胞治疗肾脏等多种疾病的临床转化也将迎来新的进展和突破。
[1] Wong C. Y. (2021). Current advances of stem cell-based therapy for kidney diseases. World journal of stem cells, 13(7), 914–933. https://doi.org/10.4252/wjsc.v13.i7.914
[2] Pang, P., Abbott, M., Chang, S. L., Abdi, M., Chauhan, N., Mistri, M., Ghofrani, J., Fucci, Q. A., Walker, C., Leonardi, C., Grady, S., Halim, A., Hoffman, R., Lu, T., Cao, H., Tullius, S. G., Malek, S., Kumar, S., Steele, G., Kibel, A., … Siedlecki, A. M. (2017). Human vascular progenitor cells derived from renal arteries are endothelial-like and assist in the repair of injured renal capillary networks. Kidney international, 91(1), 129–143. https://doi.org/10.1016/j.kint.2016.07.037
[3] Patschan, D., Schwarze, K., Henze, E., Patschan, S., & Müller, G. A. (2016). The endothelial-to-mesenchymal transition and endothelial cilia in EPC-mediated postischemic kidney protection. American journal of physiology. Renal physiology, 310(7), F679–F687. https://doi.org/10.1152/ajprenal.00306.2015
[4] Ardeshirylajimi, A., Vakilian, S., Salehi, M., & Mossahebi-Mohammadi, M. (2017). Renal Differentiation of Mesenchymal Stem Cells Seeded on Nanofibrous Scaffolds Improved by Human Renal Tubular Cell Lines-Conditioned Medium. ASAIO journal (American Society for Artificial Internal Organs : 1992), 63(3), 356–363. https://doi.org/10.1097/MAT.0000000000000470
[5] Wang, Y., He, J., Pei, X., & Zhao, W. (2013). Systematic review and meta-analysis of mesenchymal stem/stromal cells therapy for impaired renal function in small animal models. Nephrology (Carlton, Vic.), 18(3), 201–208. https://doi.org/10.1111/nep.12018
[6] Tögel, F. E., & Westenfelder, C. (2012). Kidney protection and regeneration following acute injury: progress through stem cell therapy. American journal of kidney diseases : the official journal of the National Kidney Foundation, 60(6), 1012–1022. https://doi.org/10.1053/j.ajkd.2012.08.034
[7] Swaminathan, M., Stafford-Smith, M., Chertow, G. M., Warnock, D. G., Paragamian, V., Brenner, R. M., Lellouche, F., Fox-Robichaud, A., Atta, M. G., Melby, S., Mehta, R. L., Wald, R., Verma, S., Mazer, C. D., & ACT-AKI investigators (2018). Allogeneic Mesenchymal Stem Cells for Treatment of AKI after Cardiac Surgery. Journal of the American Society of Nephrology : JASN, 29(1), 260–267. https://doi.org/10.1681/ASN.2016101150
[8] Villanueva, S., González, F., Lorca, E., Tapia, A., López, V. G., Strodthoff, R., Fajre, F., Carreño, J. E., Valjalo, R., Vergara, C., Lecanda, M., Bartolucci, J., Figueroa, F. E., & Khoury, M. (2019). Adipose tissue-derived mesenchymal stromal cells for treating chronic kidney disease: A pilot study assessing safety and clinical feasibility. Kidney research and clinical practice, 38(2), 176–185. https://doi.org/10.23876/j.krcp.18.0139
[9] Makhlough, A., Shekarchian, S., Moghadasali, R., Einollahi, B., Hosseini, S. E., Jaroughi, N., Bolurieh, T., Baharvand, H., & Aghdami, N. (2017). Safety and tolerability of autologous bone marrow mesenchymal stromal cells in ADPKD patients. Stem cell research & therapy, 8(1), 116. https://doi.org/10.1186/s13287-017-0557-7
相关新闻
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



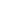
服务热线
400-885-0012


在线咨询

官方微信



TOP
