




引言
血脑屏障就像是大脑的“保安系统”。它的存在,保护了大脑免受外界侵害,但也给治疗脑部疾病带来了挑战。不过,现在科学家们正努力寻找方法,比如利用间充质干细胞穿越这道屏障,为治疗脑部疾病开辟新路径。而科学研究也发现,间充质干细胞具有独特的技能——穿越血脑屏障,这一特性就为治疗脑部等中枢系统疾病带去了新的临床用药选择,也给患者们带去了新的希望。今天我们就一起来解锁间充质干细胞“穿越血脑屏障”的技能,以及凭借这个优势,间充质干细胞开启了脑部疾病治疗的新路径。
血脑屏障(Blood-Brain Barrier,简称BBB)就像是大脑的“保安系统”。想象一下,我们的大脑是一座非常重要且精密的“城堡”,而血脑屏障就是环绕城堡的坚固城墙。
这扇屏障由紧密排列的脑细胞和它们之间的特殊结构组成。它的存在,保护了大脑免受外界侵害,但也给治疗脑部疾病带来了挑战。
在脑毛细血管内,有一个血脑屏障和内皮膜的存在[2],这就相当于在脑子和外界之间立起一道“坚不可摧的围墙”,使得许多治疗药物无法达到脑部病灶发挥作用,无法有效阻止病情恶化。
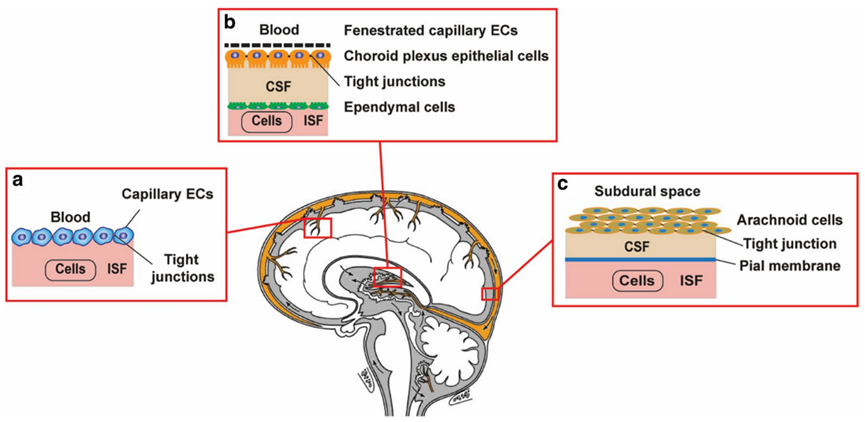
(图片来自参考文献2)
不过,现在科学家们正努力寻找方法,比如利用间充质干细胞(MSCs),希望能安全穿越这道屏障,为治疗脑部疾病开辟新路径。
在过去的几十年中,大量的证据已经证明基于干细胞的治疗在这一领域可能是有希望的,干细胞疗法可能是治疗脑部等中枢神经系统疾病的一种有前景的方法。
随着医学技术的不断发展,间充质干细胞正逐渐成为目前临床研究的热点,而基于MSCs的干细胞疗法作为再生医学疗法之一也正展现着其在治疗各种疾病中的潜力。如下图所示,MSCs不仅拥有自我更新和多向分化的能力,MSCs还能在特定条件下转化为各种不同类型的细胞,如骨细胞、脂肪细胞和神经细胞等[1]。
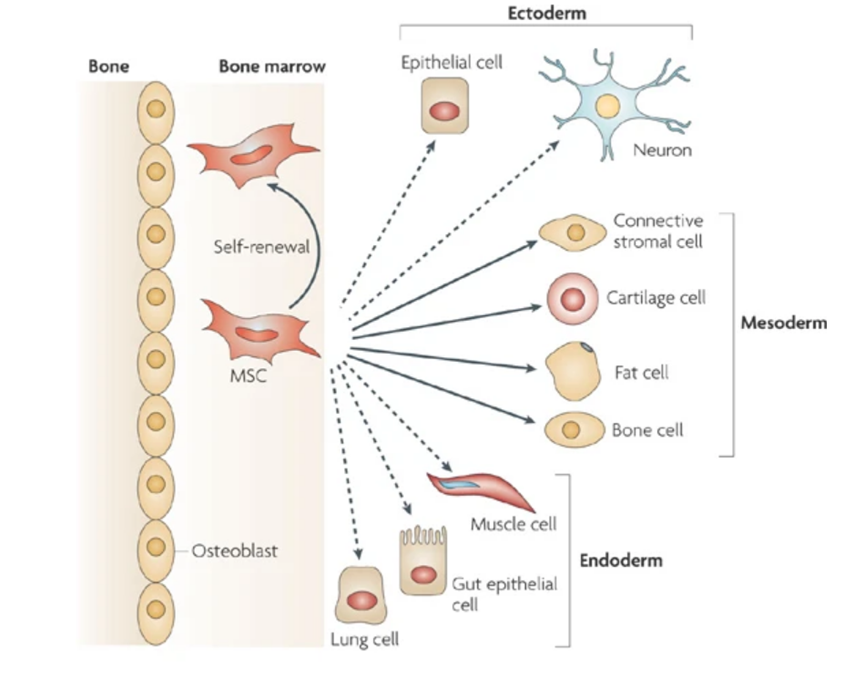
(图片来自参考文献1)
科学研究还发现, MSCs具有一项独特的“技能”——穿越血脑屏障,这一特性就为治疗脑部等中枢系统疾病带去了新的临床用药选择,也给患者们带去了新的希望。
近期,发表在“pharmaceutics”上的一篇名为“Mesenchymal Stem Cell (MSC)-Based Drug Delivery into the Brain across the Blood–Brain Barrier”的新综述[3]就重点阐述了使用MSCs作为载体穿过血脑屏障将药物递送到大脑中这一方式在脑部恶性肿瘤治疗中的优势及应用前景。

间充质干细胞是如何穿越血脑屏障的?
首先,先让我们来了解一下MSCs是怎么能够突破血脑屏障这堵“围墙”的。这一过程并非是简单通过物理穿透,而是利用了细胞间的复杂相互作用和分子机制。
下图展示的是基于间充质干细胞(MSC)的药物穿过血脑屏障进入大脑的途径。黑色圆圈代表药物、载药纳米颗粒等物质。灰色圆圈或灰色椭圆表示MSCs细胞核。
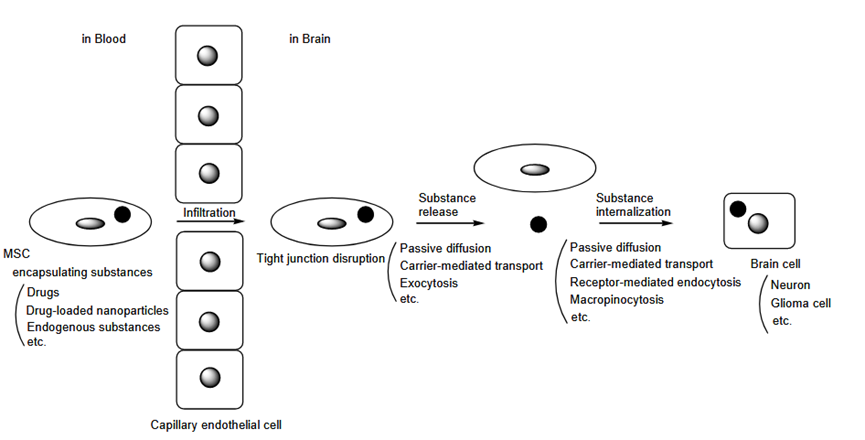
(图片来自参考文献3)
关于突破BBB的细胞间的作用机制较为复杂,就不详细展开,简而言之可以分为以下两方面。
一方面,当疾病进展时,其周围的免疫微环境分泌的细胞因子会呈“阶梯式分布”,而MSCs恰恰能够“感知”并沿着这个“梯度”去寻找受伤或病变组织发出的信号,并主动迁移到这些区域进行修复;
另一方面,根据Stephen Paget博士提出的“种子和土壤”理论[4],在外周血中的MSCs分子会与BBB处的毛细血管内皮细胞进行融合,从而破坏BBB处内皮细胞的紧密连接,进而可以进入到脑部等相应靶区发挥作用。
一旦进入大脑,MSCs就能够释放出其携带的药物或生长因子,直接作用于受损的脑细胞,促进修复和再生。
间充质干细胞治疗脑部疾病的新方式:
作为药物载体直击大脑病灶
Jianjun Ma团队等人在“Cell Death Discovery”上揭示了MSCs可以充当一个生物分子的载体,类似于“货物船”,载着miRNA、蛋白质、抗癌药物等“脆弱的货物”进入脑部等相关病灶发挥作用,进而改善帕金森样症状[5]。主要实验结果如下图所示。
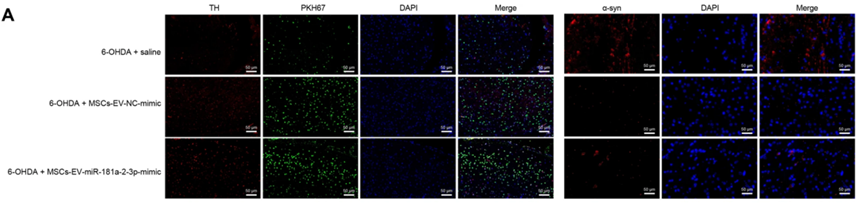
(图片来自参考文献5)
有MSC辅助运输药物的实验组相较于没有MSC辅助运输药物的对照组而言,其α-突触核蛋白(α-syn)(PD中的病理纤维)的表达水平显著降低。
利用MSCs作为药物载体,具有以下许多传统药物传递方式无法比拟的优势:
间充质干细胞作为药物载体的优势
1.高度选择性:MSCs能够精准地迁移到受损的脑组织,实现药物的精确投放,避免了全身用药可能带来的副作用;
2.高效性:MSCs在穿越血脑屏障后,能够直接释放药物到目标区域,提高了药物的生物利用度和治疗效果;
3.再生功能:除了作为药物载体外,MSCs还具有促进组织修复和再生的能力,可以进一步加速受损脑组织的恢复。
正是因为MSCs由以上优势,如下图所示,目前已经有多项临床试验是基于间充质干细胞作为药物载体应用于临床疾病的诊疗中。其中,各项研究都指出由MSCs作为载体递送的药物都准确递送到了靶位点而没有严重的脱靶副作用,这也进一步证明了MSCs在治疗脑部等中枢神经系统相关疾病中的有效性及安全性。
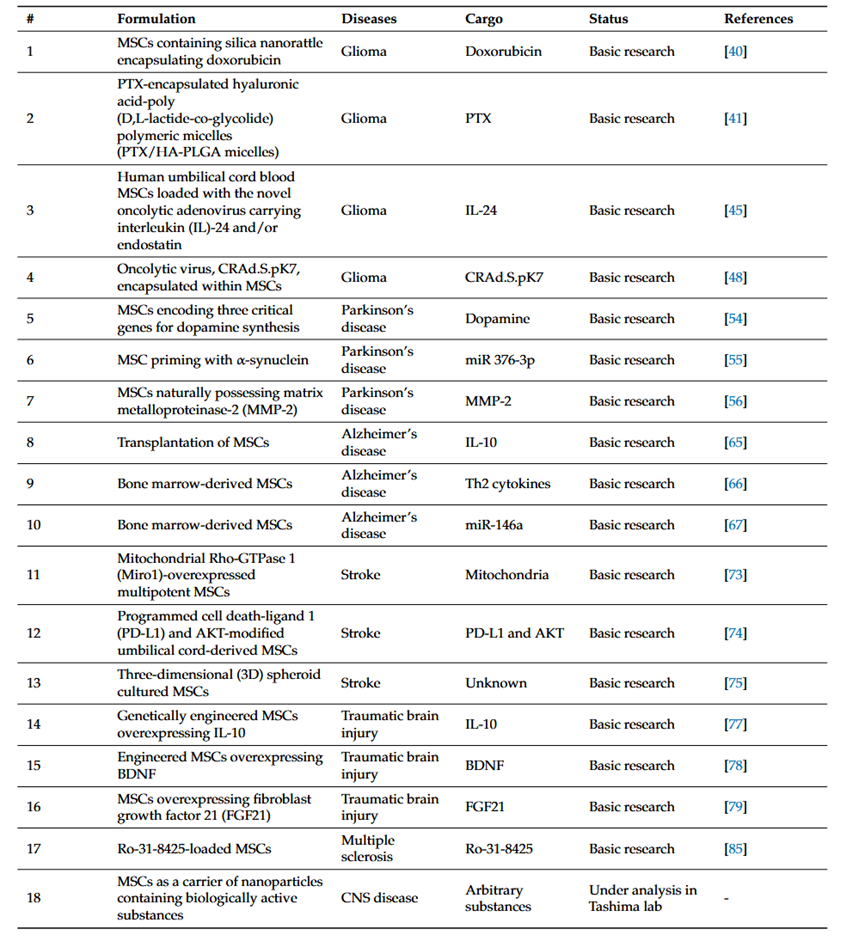
(图片来自参考文献3)
小结
目前,间充质干细胞在穿越血脑屏障方面的潜力已经被广泛认可,并在多种神经系统疾病的治疗中展现出巨大潜力。例如,阿尔茨海默病、帕金森病等神经退行性疾病,以及脑卒中等急性脑部损伤,都可能通过间充质干细胞介导的药物传递系统得到有效治疗。随着研究的不断深入和技术的不断进步,我们有理由相信,间充质干细胞将在未来的医学领域发挥更加重要的作用,为更多的患者带来健康和希望。
参考文献:
[1]Uccelli A, Moretta L, Pistoia V. Mesenchymal stem cells in health and disease. Nat Rev Immunol. 2008 Sep;8(9):726-36. doi: 10.1038/nri2395IF: 100.3 Q1 . PMID: 19172693.
链接:https://www.nature.com/articles/nri2395
[2]Kadry, Hossam et al. “A blood-brain barrier overview on structure, function, impairment, and biomarkers of integrity.” Fluids and barriers of the CNS vol. 17,1 69. 18 Nov. 2020, doi:10.1186/s12987-020-00230-3IF: 7.3 Q1
链接:https://sci-hub.st/10.1186/s12987-020-00230-3
[3] Tashima, T. Mesenchymal Stem Cell (MSC)-Based Drug Delivery into the Brain across the Blood–Brain Barrier. Pharmaceutics 2024, 16, 289.
链接:https://doi.org/10.3390/pharmaceutics16020289
[4] Paget, S. The Distribution of Secondary Growths in Cancer of the Breast. Lancet 1889, 133, 571–573.
链接:
https://integrative-cancer-care.org/wp-content/uploads/2021/11/1889-Distribution-of-secondary-growths-in-cancer-of-the-breast.pdf
[5] Ma, J., Shi, X., Li, M. et al. MicroRNA-181a–2–3p shuttled by mesenchymal stem cell-secreted extracellular vesicles inhibits oxidative stress in Parkinson’s disease by inhibiting EGR1 and NOX4. Cell Death Discov. 8, 33 (2022).
链接:https://doi.org/10.1038/s41420-022-00823-x
相关新闻
博雅新闻

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
